サプリメント事業者必見!「食品表示基準改正」のポイント・猶予期限に向けた計画的な実務対応ガイド
- 健康食品・サプリ記事(112)
- 商品開発(57)
- 関連法規(8)
- 2026.02.10

この記事で分かること
- 2025年3月施行の「食品表示基準改正」におけるサプリメント特有の重要ポイント
- 栄養強化目的の添加物表示義務化と、栄養素等表示基準値改正による具体的な影響
- 「デザイン変更」か「配合変更」か?コストを抑える実務対応の手順と優先順位の付け方
- 法改正を「単なる義務」で終わらせず、商品競争力を高めるリニューアルに繋げる戦略
2025年3月28日に食品表示基準改正が施行され、サプリメントを取り巻く表示ルールが新しくなりました。栄養強化目的の添加物表示や、2025年版の食事摂取基準に基づいた栄養成分値の改訂など、対応すべき項目は多岐にわたり、「経過措置期間をどう活用すべきか」「どのタイミングで切り替えるのが最適か」と、お悩みの企業も多いのではないでしょうか。
そこで本記事では、期限までの具体的な進め方と、この改正を機に製品の価値をさらに高めるためのヒントを、実務ご担当者向けにわかりやすく解説します。
食品表示基準改正2025年3月版の重要ポイント
サプリメント業界に影響のある改正内容は以下の通りです。
商品パッケージやラベルの記載事項に影響する変更点が、多く含まれています。
- 栄養強化目的で使用した食品添加物の表示の義務化
- 栄養素等表示基準値等の改正
今回の改正は法的義務ですが、「健康意識の高い消費者視点に寄り添った」改正であることがポイントです。
そのため、新たな基準に即した商品開発・既存品リニューアルにより、競争力向上や新規顧客獲得も可能です。
ここからは、適切な対応を進める上でのポイントを、詳しく解説します。
①栄養強化目的で使用した食品添加物の表示の義務化
これまでサプリメントなどの「栄養強化目的で使用した食品添加物」は、特別用途食品や機能性表示食品を除き、表示義務が免除されていました。しかし、今回の改正施行により表示が必要となります。
対象:ビタミン類、ミネラル類、アミノ酸類などの栄養強化剤として使用される食品添加物
たとえば、ビタミンCを栄養強化目的として配合した顆粒の青汁製品の場合、これまではビタミンCの表示は省略が可能でしたが、今後は原材料名として「ビタミンC」の表示が必要になります。
例)ビタミンCを栄養強化目的で配合した商品の原材料名表示
| 改正前 | 原材料名:大麦若葉末(国内製造)、デキストリン/卵殻カルシウム |
|---|---|
| 改正後 | 原材料名:大麦若葉末(国内製造)、デキストリン/卵殻カルシウム、ビタミンC |
経過措置期間:2030年3月31日までに製造・加工・輸入された商品については改正前の表示でも販売可能
*OEMメーカーと配合内容を確認し合い、配合変更や表示変更を進める具体的な実行計画が必要です。
②栄養素等表示基準値等の改正
日本人の食事摂取基準(2025年版)に基づく「栄養素等表示基準値」の全面的な見直しも行われています。
複数の栄養素で基準値が変更され、たとえば、ビタミンB12が2.4µgから4.0µgへ、ビタミンDも5.5µgから9.0µgへと大幅に増加。商品に「1食分のビタミンB12を摂取できる」「1日分のビタミンを摂取できる」といった表現があれば、修正が必要です。
経過措置期間:2028年3月31日製造分まで
| 栄養素 | 単位 | 現行 | 改正 |
|---|---|---|---|
| たんぱく質 | g | 81 | 85 |
| 脂質 | g | 62 | 70 |
| 飽和脂肪酸 | g | 16 | 17 |
| n-6系脂肪酸 | g | 9.0 | 10.0 |
| 食物繊維 | g | 19 | 20 |
| 亜鉛 | mg | 8.8 | 8.5 |
| カルシウム | mg | 680 | 700 |
| 鉄 | mg | 6.8 | 6.5 |
| 銅 | mg | 0.9 | 0.8 |
| ナトリウム | mg | 2900 | 2700 |
| (食塩相当量) | g | なし | 7.0 |
| マンガン | mg | 3.8 | 3.2 |
| ヨウ素 | μg | 130 | 140 |
| パントテン酸 | mg | 4.8 | 5.5 |
| ビタミンB1 | mg | 1.2 | 1.0 |
| ビタミンB12 | μg | 2.4 | 4.0 |
| ビタミンD | μg | 5.5 | 9.0 |
| ビタミンE | mg | 6.3 | 6.5 |
赤文字:基準値増加(より多くの含有量が必要)、青文字:基準値減少(より少ない含有量で表示可能)
強調表示の変更
たとえばビタミンB12は基準値が増加するため、「ビタミンB12を含む」「ビタミンB12高配合」といった表現があれば、新基準では表示基準を満たさない可能性が出てきます。
一方で、ビタミンB1は基準値が減少するため、より少ない配合量でも「高配合」や「たっぷり」等の強調表示が可能になります。健康食品メーカー・ブランドオーナーの皆様は、自社商品の配合量と新基準値を照らし合わせて、必要に応じて表示内容の見直しが必要です。
経過措置期間:2028年3月31日製造分まで
| 栄養成分 | 単位 | 含む旨 (100g当たり) |
高い旨 (100g当たり) |
強化された旨 (100g当たり) |
|||
|---|---|---|---|---|---|---|---|
| 現行 | 改正 | 現行 | 改正 | 現行 | 改正 | ||
| たんぱく質 | g | 8.1 | 8.5 | 16.2 | 17.0 | 8.1 | 8.5 |
| 亜鉛 | mg | 1.32 | 1.28 | 2.64 | 2.55 | 0.88 | 0.85 |
| カルシウム | mg | 102 | 105 | 204 | 210 | 68 | 70 |
| 鉄 | mg | 1.02 | 0.98 | 2.04 | 1.95 | 0.68 | 0.65 |
| 銅 | mg | 0.14 | 0.12 | 0.27 | 0.24 | 0.09 | 0.08 |
| パントテン酸 | mg | 0.72 | 0.83 | 1.44 | 1.65 | 0.48 | 0.55 |
| ビタミンB1 | mg | 0.18 | 0.15 | 0.36 | 0.30 | 0.12 | 0.10 |
| ビタミンB12 | μg | 0.36 | 0.60 | 0.72 | 1.20 | 0.24 | 0.40 |
| ビタミンD | μg | 0.83 | 1.35 | 1.65 | 2.70 | 0.55 | 0.90 |
| ビタミンE | mg | 0.95 | 0.98 | 1.89 | 1.95 | 0.63 | 0.65 |
赤文字:基準値増加、青文字:基準値減少
食物繊維のゼロ表示規定と栄養成分測定方法の変更点
サプリメント業界に影響のある改正内容ではありませんが、食品100gあたりの食物繊維含有量が0.5g未満の場合、「0(ゼロ)」と表示することが可能となりました。これまで明確な基準がなかった食物繊維のゼロ表示について、初めて具体的な規定が設けられました。
また、ビタミンB群の測定方法に高速液体クロマトグラフ法が追加され、より正確な栄養成分表示ができるようになりました。
改正対応のタイムラインと具体的な実務手順
今回の改正では、項目ごとに経過措置期間が異なります。施行後3年から5年の比較的長い期間が設定されています。しかし、パッケージデザインの再検討や配合変更、既存資材の在庫調整やシール貼り作業などには、相応の時間が必要です。
アイテムごとに計画的に対応することで、コストの抑制と確実な法令遵守が、両立できます。
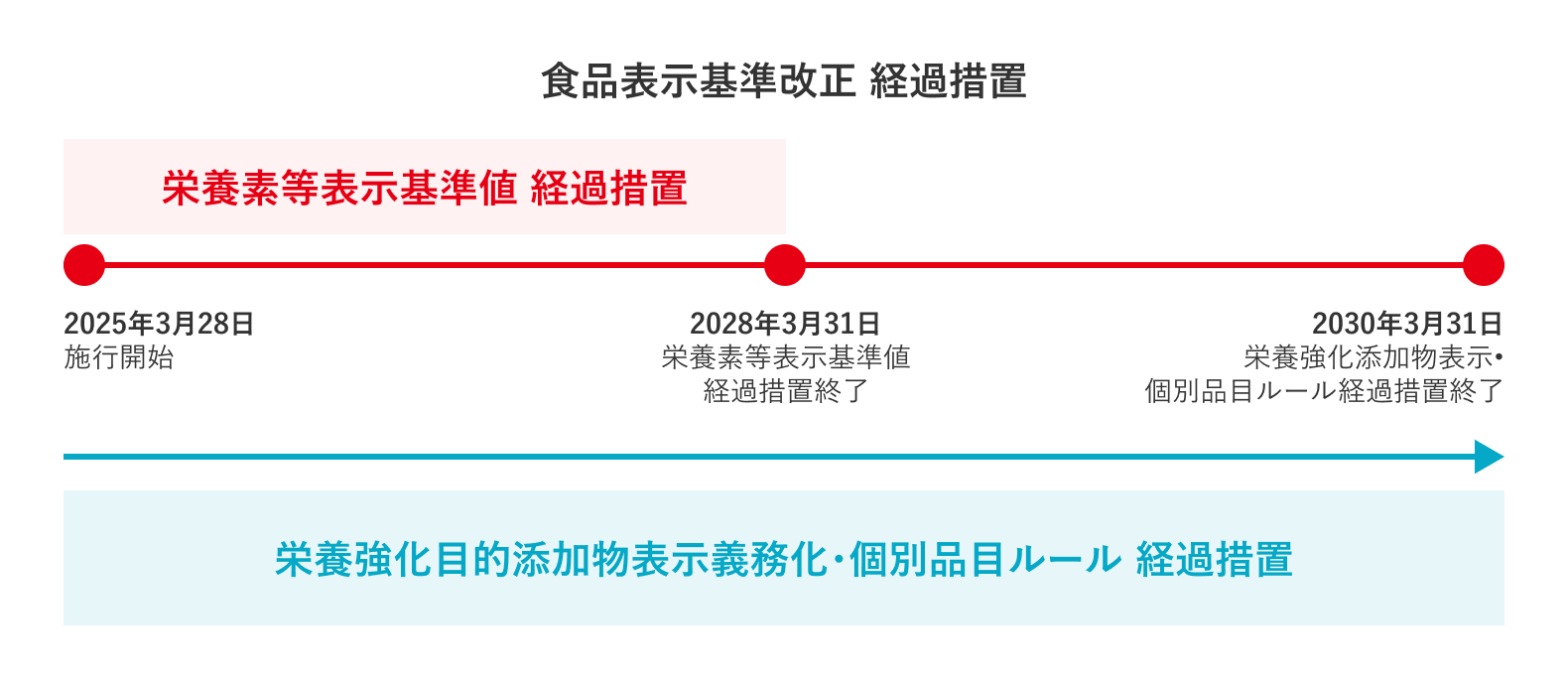
施行期日と経過措置期間
自社商品がどの改正項目に該当するかを早期に確認し、優先順位をつけて対応計画を立てましょう。
- 栄養強化目的で使用した食品添加物の表示の義務化
2030年3月31日製造分までは、改正前の基準でも可能な長めの経過措置期間 - 栄養素等表示基準値等の改正
2028年3月31日製造分までは、改正前の基準でも可能な経過措置期間
改正への対応
対応としては、まず「現在の表示内容は、今回の改正で影響が生じるか?」の確認から始めましょう。
改正該当箇所を特定した上で、
- デザイン変更(改版)
- 配合変更
のどちらで対応するかを、決定しましょう。
A)デザイン変更(改版)の場合
パッケージ自体を新たに印刷し直すのか、既存パッケージの在庫にシール対応するのかにより、費用が変わります。既存包材・シールの在庫との兼ね合いを考慮し、OEMメーカーと計画的な切り替えを相談しましょう。
- 現行のパッケージやラベルの改正該当箇所を特定する
- 新表示内容を確定する
- デザインを修正する
- 印刷会社に発注する
B)配合変更の場合
配合変更はAの表示修正に比べ、開発や品質管理、調達など多部門にまたがる対応が必要となります。スケジュールやコストへの影響も大きいため、早めの検討・準備が重要です。
- 現行の配合(原材料の種類や配合割合)における影響箇所を特定
- 改正によって新たに表示義務が生じる成分/使用制限が設けられた原材料がないかを確認
- 必要に応じて配合を見直す
- 新たな表示規制に適合させる、または新たなニーズ・ターゲット層をとらえた配合調整を検討
- 場合によっては、代替原料の選定が必要となることも
- 新たな配合での試作・品質確認を行う
- 新たな配合で製品を試作、品質や安全性、味・食感などの確認を行う
- 新たな配合に基づく表示内容を作成する
- 新しい原材料や配合割合に合わせ、食品表示内容を作成・修正
- 関係各所への連絡・調整
- OEMメーカーや原材料サプライヤー、品質管理部門などと連携し、スムーズな切り替えを図る
栄養成分分析の再実施タイミング・優先順位の決定方法
「栄養成分分析の再実施」が必要な商品を特定するためには、改正内容と現在の分析値の照合から始めましょう。
栄養素等表示基準値の変更によって配合を変更した商品は、新たに栄養成分分析を行う必要があります。
対象商品が多くある場合には、優先順位を決定する必要があります。
優先順位の付け方の例
- 文部科学省の食品成分委員会が「日本食品標準成分表」の改訂や分析対象食品の選定に関して、優先順位付けの考え方を資料で示しているものを参考に、①利用頻度・重要性、②新規性、③流通・消費状況を評価する
- 売上高上位商品かつ栄養強調表示を行う商品から着手することもあれば、逆にこのような商品はできる限り遅らせる判断もある。実際のビジネスに応じて優先順位を決める
具体的には、ビタミンB12やビタミンDなど基準値が大幅変更された成分を配合する商品、「食物繊維のゼロ表示」を検討する商品を優先することをお勧めします。
また、分析コストを抑えるために類似配合の商品はグループ化して対応することも検討しましょう。
改正対応の社内体制と関連部署の役割
今回の食品表示基準改正に効率的に対応するには、会社の規模によってはプロジェクトチームの立ち上げを検討しましょう。スタートアップでOEMメーカーに任せているなど、組織規模により例外はありますが、以下のようなチーム構成がお勧めです。
- 品質管理部門:改正内容の解釈と対応方針の策定
- 商品開発部門:配合変更の要否を判断・必要があれば配合変更
- 生産管理部・製造委託している窓口部門:製造にどのような影響があるかを評価
- 法務部門:規制の解釈をサポート、対応内容によってはリスク評価を実施
- 営業販売部門:顧客への説明資料の作成、問い合わせ対応窓口
サプリメントメーカーの実務対応
中小規模の事業者の課題は、「今回の改正への対応を限られたリソースでいかに行うか」ということです。
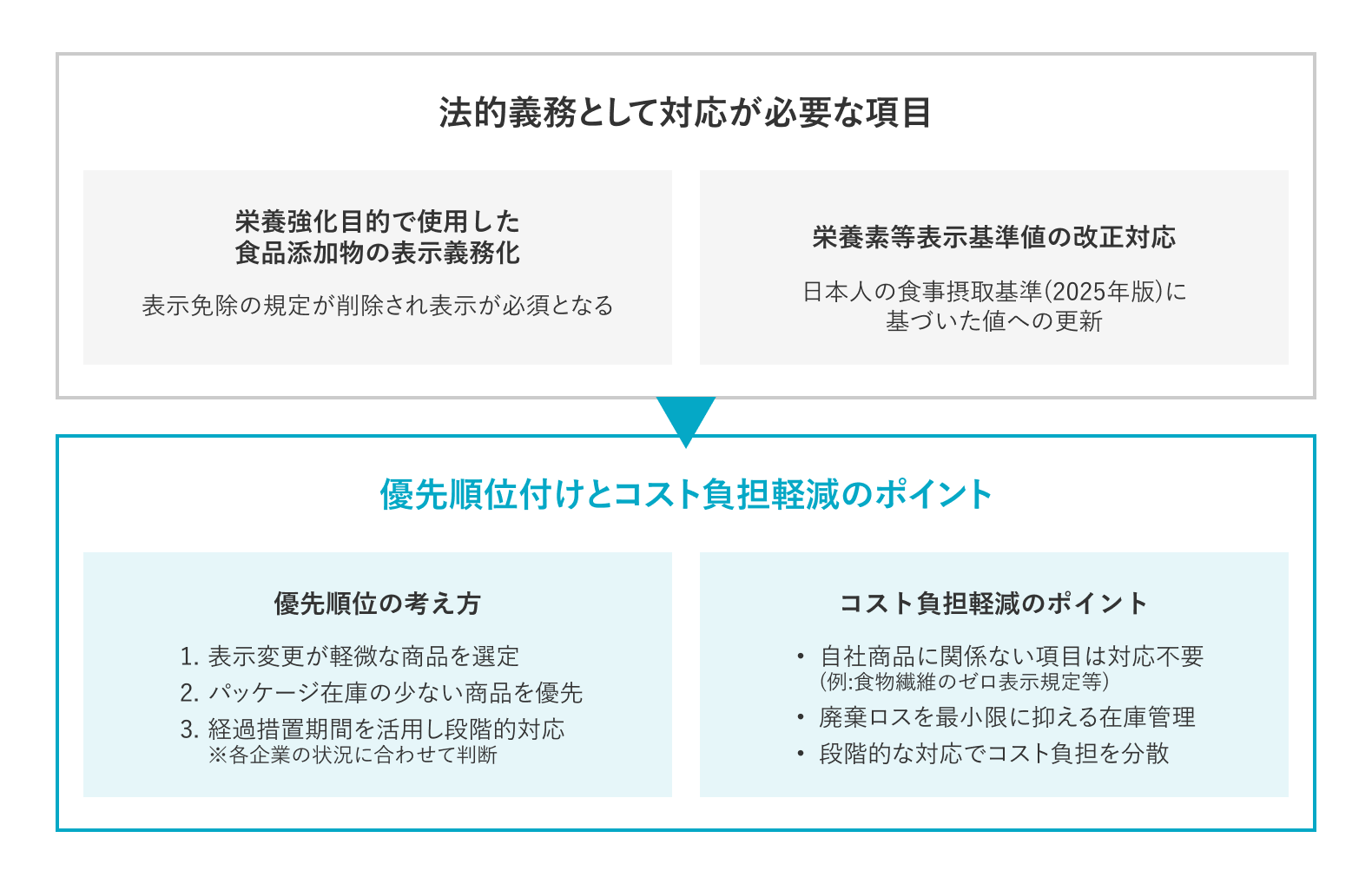
対応必須項目と猶予可能項目の判別法と優先順位付け
限られた予算・人員で効率的に進めるためには、「対応必須項目と猶予可能項目の判別」が求められます。
- 法的義務として速やかに対応が必要:栄養強化目的で使用した食品添加物の表示義務化/栄養素等表示基準値の改正対応
- 対応不要:食物繊維のゼロ表示規定など、自社商品に該当しない項目
経過措置期間を活用し、段階的な対応計画を策定することで、負荷を分散できます。
原料サプライヤーから入手すべき情報
改正対応を効率的に進めるために、原料サプライヤーから適切な情報を収集することが不可欠です。
実際に、サプライヤーとの情報共有不足が原因で、対応が後手に回るケースが増えており注意が必要です。
まず入手すべきものは、「原料の正確な栄養成分分析値」と「分析証明書」です。
特に栄養強化目的で使用される添加物については、配合量の根拠となるデータが必要となります。
製造委託している場合は、委託先のOEMメーカーが原料サプライヤーから集めてくれます。
信頼できるOEMメーカーの選定は、法令遵守と品質向上のためにとても重要です。
そのため、OEMメーカーの選定では「製造実績」に加えて、「法規制への迅速な対応力とサポート体制」を評価し、「長期的なパートナーシップが築けるか?」という視点が大切です。
改正対応を新たなビジネスチャンスに活かすには?

前述の通り、今回の食品表示基準改正対応は、新たな機会の創出に活かすことができます。
ここではその実例を紹介します。
食品表示基準改正を、新たな差別化のチャンスと捉える
- 新たな基準に即した商品開発や既存品のリニューアルを実施
- ターゲット層の情報更新、商品コンセプトの刷新を行い、新規顧客の獲得へつなげる
改正によって義務化された栄養強化目的の添加物表示をアピール材料として活用する
- たとえばビタミンCを栄養強化目的で配合した商品では、従来は表示されなかった添加物が明記されることで、消費者に「実際にビタミンCが配合されている」という安心感が提供可能に
- 栄養素等表示基準値の改正により、従来より少ない配合量で栄養強調表示が可能になる成分もあるため、コストメリットのある商品開発にもつなげることが可能
このように、改正対応は単なる義務ではなく、商品価値向上の機会として位置づけることが重要です。
今後予想される規制動向と対応準備
今回の食品表示基準改正に続き、今後は「ステルスマーケティング規制の強化」や「ダークパターンに対する新たな規制」などが予想されます。さらに、消費者庁による「機能性表示食品制度のさらなる見直し」も想定されます。
いずれにせよ、エビデンスの質向上と透明性確保に備えた商品開発が、結果的に競争力を生む源泉であることに変わりはありません。さらに、日頃から業界情報や行政の動向などについての情報収集を欠かさないことが大切です。OEMメーカーとの戦略的なパートナーシップが、これまで以上に重要になるでしょう。
まとめ
いかがでしょうか。食品表示基準の改正対応は、単なる法令遵守にとどまらず、お客様へ商品の魅力を正しく、より誠実にお伝えする大切なプロセスであり、差別化につながる絶好の好機でもあることが、お分かりいただけたでしょうか。
2028年・2030年の経過措置終了を見据え、早めに準備を進めることで、包材の廃棄コストを抑えつつ、余裕を持ったリニューアルが可能になります。
東洋新薬では、最新の規制動向に基づいた表示のご提案はもちろん、新基準に即した配合の最適化など、商品の価値をさらに引き出すお手伝いをさせていただきます。現在の表示に関する些細な疑問からでも、ぜひお気軽にご相談ください。

東洋新薬は健康食品・化粧品業界を陰で支えるODEM(ODM&OEM)メーカーとして、世界の人々の『健康と美』への期待に『価値』で応えていくことをミッションとしています。 本サイトでは通販ビジネスにかかわるすべての皆様に様々な情報をお届けしています。
関連情報

機能性表示食品の商品開発を例に、健康食品・サプリメントのOEM製造の流れを細かくまとめた資料です。お客様側とOEM側のそれぞれの対応や注意点などをご紹介します。
関連記事
-
1

- 「保健機能食品制度」とは?
- 健康食品・サプリ記事
- 関連法規
-
2

- 消費者庁 機能性表示食品 事後チェック指針 とは?
- 健康食品・サプリ記事
- 関連法規
-
3
- 健康食品と栄養成分表示について。消費者の関心が高い成分とは?
- 健康食品・サプリ記事
- 関連法規
-
4

- 食品表示法とは?表示が義務化された「栄養成分表示」
- 健康食品・サプリ記事
- 関連法規
-
5

- サプリメント事業者必見!「食品表示基準改正」のポイント・猶予期限に向けた計画的な実務対応ガイド
- 健康食品・サプリ記事
- 商品開発
- 関連法規
-

- 製剤技術「イージーパウダー®」のご紹介
-

- スタートアップ企業必見!20代~40代向け 青汁 OEM商品開発の成功ポイント
-

- 【2025年最新】食品表示における「製造所固有記号」とは?― その目的と取得の方法
-

- 開発実績多数あり!「免疫ケアタブレットOEM CRL1505乳酸菌」の商品カタログ資料
-

- Wellness Daily News 健康食品 Inside Out 大麦若葉青汁ができるまで
-

- Wellness Daily News サプリ製造の現場から 東洋新薬品質保証編/工場内部へ
-

- インドマンゴスチンエキス末のご紹介
-

- CRL1505乳酸菌のご紹介
-

- 開発実績多数あり!「インドマンゴスチン脂肪・BMIケアタブレットOEM」の商品カタログ資料
-

- 開発実績多数あり!「溶けやすいプロテイン粉末飲料OEMイージーパウダー®」の商品カタログ資料
-

- 商品開発担当者向け 機能性表示食品届出の「3つの壁」~事例から見たその回避術
-

- 開発実績多数あり!「飲みこみやすいイージータブ® ブラックジンジャーサプリメント」の商品カタログ資料
-

- 健食・化粧品商品開発専用スペース「クイックラボ渋谷(QLS)」のご案内
-

- OEM 商品企画~製造の流れガイド~【健康食品・サプリメント編】
-

- 黒ショウガエキス末のご紹介
-

- 「売れる青汁」は主原料に注目!差別化商品を生み出す5つのポイント
-

- コロナ禍で市場拡大? 市場データと事例から見る「青汁」商品開発のヒント
-

- 機能性表示食品 免疫ケアタブレットCRL1505乳酸菌
-

- 機能性表示食品 脂肪・BMIケアタブレット
-

- 溶けやすいプロテイン粉末飲料
-

- イージータブサプリメント
-

- オーラルケアタブレット
-

- 特保の青汁
-

- 機能性表示 ダイエットサプリ