化粧品の「医薬部外品」とは?OEM開発時のメリット・デメリットと注意点
- 2021.03.12

化粧品の容器/パッケージの「医薬部外品」「薬用」という記載。この意味するところ、理解していますか?今回は、「化粧品」「医薬部外品」「薬用化粧品」の違いと、「医薬部外品」のメリット・デメリット、そしてOEM開発時の注意点などを解説します。
医薬部外品は消費者からの注目度も高く、商品訴求力アップの可能性を秘めていますので、今回ご紹介するメリット・デメリットを理解し、リスクのない商品開発を行いましょう。
「医薬部外品」とは?化粧品や薬用化粧品との違い
「医薬部外品」とは日本の医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下、薬機法)に定められた、医薬品と化粧品の中間的な分類です。
「医薬品」と「化粧品」の間に位置づけられ、医薬品が病状の改善を目的としているとすると、医薬部外品の目的はあくまで「予防」です。そのため、医薬部外品は作用が穏やかで、化粧品と同様、使用して副作用があってはいけません。
>関連情報:一般的な化粧品と医薬部外品の違いを教えてください~医薬部外品化するメリットとデメリット~
医薬部外品の代表的な例として育毛剤や染毛剤、パーマ剤や薬用歯磨き粉などがあります。医薬部外品の中には、石けんや化粧水、美容液などの薬用化粧品も含まれます。
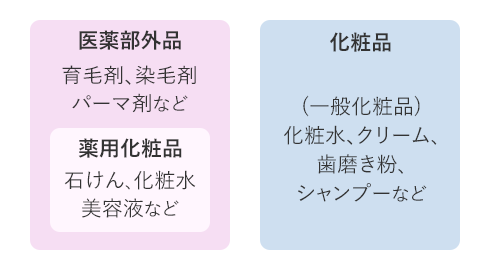
化粧品と法律
化粧品を製造、または販売するにあたり、消費者の安全性を守ることを目的として、さまざまなルール(法律や業界の自主基準、ガイドライン)が厳密に定められています。
そもそも「化粧品」とは何でしょうか?化粧品とは、「人体に対する作用が緩和なもので容貌を変え、又は皮膚もしくは毛髪をすこやかに保つためのもの」と法律で定められています*1。すこし難しいのでもう少しシンプルに説明すると「副作用がなく、安全に肌や髪を健康に保つもの」が化粧品です。スキンケア品やメークアップ品、シャンプーやトリートメント、ネイルケア品、歯磨き粉なども化粧品に分類されます。
では、「医薬部外品」とは何でしょうか?医薬部外品は、化粧品と医薬品の間に位置し、「有効成分」が配合されている製品を指します。また、薬用ローションや薬用石けん・薬用シャンプーなどの「薬用化粧品」と呼ばれるものも、医薬部外品の中に含まれます。
 【出典:日本化粧品工業連合会 化粧品用語解説 化粧品と薬用化粧品】
【出典:日本化粧品工業連合会 化粧品用語解説 化粧品と薬用化粧品】
*1「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」
化粧品と医薬部外品の大きな違い「有効成分」とは?

前述の通り「医薬部外品」とは化粧品と医薬品の間に位置し、「有効成分」が配合されている製品を指します。「有効成分」とは、安全性や有効性などさまざまな試験をクリアした特定の肌悩みに対して効果効能があると厚生労働省に認められた成分のことです。
有名なものでは、美白作用が期待できる「ビタミンC」や「アルブチン」「トラネキサム酸」などが挙げられます。処方面においてはこの有効成分の有無が、化粧品と医薬部外品の最大の違いです。
「医薬部外品」のメリット・デメリット
「医薬部外品」は承認を受けた有効成分に紐づいた効能効果を、製品のパッケージに明記できます。たとえば、化粧品はスキンケア商品において「美白」という表現はできませんが、美白の有効成分を配合している医薬部外品であれば、「メラニン生成を抑え、シミそばかすを防ぐ」と表現可能です。薬用洗顔料で殺菌剤が含まれるものは「皮膚の洗浄や殺菌」「体臭を防ぐ」という記載が認められます。最近では「シワ改善」という効能効果の製品も新たに登場しています。
このように「医薬部外品」は消費者の悩みに沿ったアピールがしやすい、というメリットがあります。
一方、デメリットは何でしょうか。それは、開発の際に選択可能な成分候補が、化粧品と比べ半減することです。有効成分以外の添加剤としての配合も、化粧品で使える成分がすべて医薬部外品でも配合できる訳ではありません。医薬部外品として配合するためには、医薬部外品としての規格を保有している原料である必要があります。そのため、新しく開発された原料やユニークな原料は「医薬部外品」では使えないことが多くあります。
<商品紹介イメージ>

「医薬部外品」の管轄機関と申請の流れ
「化粧品」と「医薬部外品」では管轄機関も異なります。
・化粧品:製造販売元の都道府県に化粧品製造販売届書の届出が必要
化粧品の届出は、各都道府県の知事宛てに「化粧品製造販売届書」と呼ばれる書類を提出します。書類の内容は商品の販売名と製造所が主で、成分に関わる情報は含まれません。
・医薬部外品:厚生労働省に、医薬部外品製造販売承認申請書の申請、承認が必要
一方「医薬部外品」は厚生労働大臣の承認が必要です。有効成分をはじめとした成分の情報、また製造方法に関わる情報も準備が必要で、よりテクニカルな内容となります。
「医薬部外品」の申請を簡単にまとめると、以下の流れとなります。
- 1. 医薬部外品に使用できる原料(成分)なのかを安全性や過去に使用された履歴などから調査を行う。
- 2. 香料なども含め、処方内容すべてを確定する。
- 3. その後、申請に必要な書類の準備に入る(申請書類は、使用原料に関する情報から製造に関わる内容まで多岐にわたる)。
- 4. 使用方法・配合成分などが過去に前例のない場合、別途資料の提出が必要になることがある。
- 5. 書類がすべて整うと、厚生労働省へ書類を提出。
- 6. 提出後、一定期間(3か月程度)が経つと、照会事項と呼ばれる厚生労働省からの問い合わせが入る場合がある。この照会事項への対応も医薬部外品申請ではキーポイントとなり、新規性が高い場合は、幾度となく照会事項が繰り返されることもある。
- 7. 照会事項がすべてクリアになると、部外品申請が承認される(処方が確定してから、承認されるまで最短でも半年程度)。
医薬部外品OEMに必要な期間と費用(コスト)とは
医薬部外品のOEM開発には、どれくらいの期間や費用(コスト)がかかるのか、気になるところですよね。
期間に関しては、医薬部外品を自社のメーカーで販売するためには厚生労働省の許可が必要なため、平均1年程度かかります。
費用(コスト)についてはさまざまな要因により変動するため、なかなか一概には言えませんが、医薬部外品は製造コストに加えて、厚生労働省申請する費用が必要になります。ただし、OEM会社が保有する既存の処方をそのまま使用する場合はこの申請費用は不要ですので、費用をおさえて短期間で商品化したい場合は、OEM会社に承認済み処方を持っているか、ご相談ください。
また、OEM会社には工場を持たないファブレスメーカーもあります。工場を所有している、製造を外注しているかで費用はもちろんやり取りに必要な時間も変わってきますので、あらかじめ確認しておくことをお勧めします。
>関連情報:ファブレスor自社工場?OEMメーカーの違いや選び方
>関連記事:化粧品OEMが売れない理由とは|選ばれる商品開発のコツ
まとめ
いかがでしょうか。東洋新薬では、医薬部外品の豊富な実績とノウハウがあり、申請済み処方も複数保有しています。短期間で医薬部外品の商品化を行いたい場合や、初めての医薬部外品の商品開発をご検討の方、化粧品よりも高いハードルを感じられて不安な方は、ぜひ東洋新薬にご相談ください。
>関連情報:化粧品OEM開発 サービスページ
>関連情報:炭酸パックOEM「一剤式高濃度炭酸パック」
>関連情報:医薬部外品OEMの商品例「オールインワンジェル」
>関連情報:医薬部外品OEMの商品例②「保湿クリーム」

東洋新薬は健康食品・化粧品業界を陰で支えるODEM(ODM&OEM)メーカーとして、世界の人々の『健康と美』への期待に『価値』で応えていくことをミッションとしています。 本サイトでは通販ビジネスにかかわるすべての皆様に様々な情報をお届けしています。
関連情報

東洋新薬では化粧品の医薬部外品OEMに対応しています。
この資料では当社で対応可能な有効成分や開発期間など医薬部外品に強い理由をご紹介しています。
関連記事
-

- 開発実績多数あり!「メイクアップベース」の商品カタログ資料
-

- 開発実績多数あり!「ビタミンC美容液」の商品カタログ資料
-

- 東洋新薬 化粧品OEM/ODMのご案内
-

- 開発実績多数あり!「ブライトニング美容液」の商品カタログ資料
-

- 開発実績多数あり!「まつ毛美容液」の商品カタログ資料
-

- 化粧品OEM開発のお悩み解決!vol.4
-

- 化粧品OEM開発のお悩み解決!vol.3
-

- 健康食品・化粧品 商品開発専用スペース クイックラボ渋谷(QLS)開設!
-

- 化粧品OEM開発のお悩み解決!vol.2
-

- 化粧品OEM開発のお悩み解決!Vol.1
-

- OEM 商品企画~製造の流れガイド~【化粧品編】
-

- 健食・化粧品商品開発専用スペース「クイックラボ渋谷(QLS)」のご案内
-

- メイクアップベース
-

- “純“ビタミンC美容液
-

- 美容液クレンジング
-

- 低刺激 保湿クリーム
-

- 三相乳化ノンケミUV
-

- うるおいハンドクリーム
-

- 高機能クッションファンデーション
-

- ブライトニング美容液
-

- まつ毛美容液
-

- アウトバストリートメント
-

- 化粧水
-

- リップエッセンス
-

- マルチ美容オイル
-

- ノンシリコンシャンプー
-

- クレイ配合洗顔フォーム
-

- 薬用育毛剤
-

- シワ改善保湿クリーム
-

- オールインワンジェル
-

- 高濃度炭酸パック